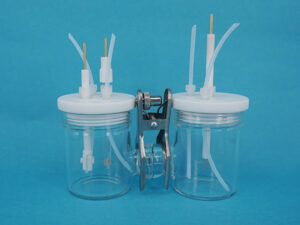
الکترود کار، کمکی و رفرنس
الکترودها در علم الکتروشیمی نقش بسیار مهمی دارند. این اجزا مهم برای انجام و اندازهگیری واکنشهای الکتروشیمی استفاده میشوند و از آنها برای اندازهگیری ولتاژ و جریان الکتریکی استفاده میشود. انواع الکترود در الکتروشیمی شامل موارد زیر است:
-
الکترود کار
-
الکترودمرجع
-
الکترود کمکی
{برای مطالعه دلایل استفاده از هرکدام از این الکترودها در سل دو و سه الکترودی کلیک کنید.}
انتخاب الکترود کار
الکترود کار ایده آل یک سطح فلزی بسیار تمیز با یک هندسه کاملاً مشخص است که در تماس مستقیم با محلول آزمایش الکتروشیمیایی است. الکترودهای کاری که برای کارهای عمومی در نظر گرفته شده اند معمولاً از فلزی ساخته می شوند که از نظر الکتروشیمیایی در طیف وسیعی از پتانسیل ها بی اثر است
پرکاربردترین فلزات در این زمینه:
- جیوه،
- پلاتین،
- طلا
- اشکال مختلف کربن
(شما میتوانید الکترود مورد نظر خود را از ما بخواهید.)
فلزات جامد معمولاً به دیسک هایی تبدیل می شوند که توسط یک پوشش شیمیایی بی اثر از تفلون، شیشه یا اپوکسی احاطه شده اند.
جیوه که یک مایع است، تمایل دارد به عنوان یک قطره کروی در تماس با محلول استفاده شود. مزایا و معایبی در رابطه با هر نوع ماده الکترود کار وجود دارد و هر کدام با جزئیات در زیر مورد بحث قرار می گیرند.
اندازه و شکل سطح الکترود
اندازه و شکل سطح الکترود نیز بر پاسخ ولتامتری الکترود تأثیر دارد.
- 1.ماکروالکترودها:
جریان کلی مشاهده شده در یک الکترود مستقیماً با مساحت سطح آن مرتبط است و الکترودهای دیسکی شکل با قطرهای بیشتر از 100 میلی متر یا ماکروالکترودها معمولاً جریان هایی را به راحتی در محدوده میکروآمپر تا میلی آمپر تولید می کنند.

- 2.میکرو الکترودها:
الکترودهایی با ابعاد کمتر از 100 میلیمتر معمولاً میکروالکترود نامیده میشوند و معمولاً جریانهایی در محدوده پیکوآمپر تا نانوآمپر تولید میکنند. اگرچه جریان کلی مشاهده شده در میکروالکترودها به اندازه کافی کوچک است وبه تجهیزات الکتروشیمیایی تخصصی نیاز دارد، این الکترودها از نسبت سیگنال به پس زمینه بیشتری برخوردار هستند و به دلیل کوچک بودن، در کاربردهایی که اندازه نمونه بسیار کوچک است کاربرد دارند.

انواع الکترود کار
- الکترود جیوه
- الکترود پلاتین
- الکترودهای طلا
- الکترود کربن
- الکترود دوار
الکترود جیوه
پلاروگرافی کلاسیک که در اکثر کتاب های درسی در مقطع کارشناسی توضیح داده شده است، از جیوه مایع به عنوان الکترود کار استفاده می کند.
- 1.(ِDME)
در متداولترین شکل آن (ِDME)، با افتادن الکترود جیوه ،مخزن جیوه آرام آرام از طریق یک لوله مویین عمودی غوطهور در محلول آزمایش الکتروشیمیایی تخلیه میشود.
هنگامی که جیوه به آرامی از مویرگ خارج می شود، قطره کوچکی با شکل تقریباً کروی تشکیل می دهد که در تماس با محلول آزمایش است. آنالیت های الکترواکتیو در محلول آزمایشی در سطح قطره تحت واکنش های اکسیداسیون یا کاهش قرار می گیرند.
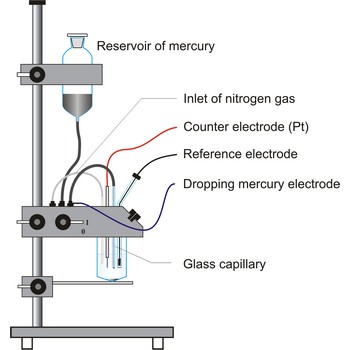
این پیکربندی الکترود از چندین مزیت برخوردار است از جمله:
مزیت های الکترود جیوه :
-
سابقه طولانی استفاده
-
سطح الکترود به راحتی قابل تکرار است . در واقع، در صورتی که سطح قطره جیوه رسوب کرد، قطره به سادگی در محلول آزمایشی ریخته می شود و یک قطره تازه در خروجی لوله مویرگی تشکیل می شود.
-
در محلولهای آبی، الکترود جیوه را میتوان در پتانسیلهای منفیتری نسبت به سایر فلزات بدون تداخل کاهش یون هیدرونیوم استفاده کرد.
-
در نهایت، الکترود جیوه نقش مهمی در استریپینگ ولتامتری ایفا می کند. تکنیکی که متکی بر پیش تغلیظ کردن یک یا چند آنالیت در الکترود جیوه و سپس الکترولیز کردن هر آنالیت از الکترود است.
معایب الکترود جیوه :
بزرگترین نقطه ضعف الکترود جیوه سمی بودن آن است. دانشجویان باید از قبل در مورد خطرات مرتبط با جیوه آگاه شوند، و باید برای جمعآوری و دفع مناسب جیوه مورد استفاده در طول آزمایش آموزش دیده باشند. علاوه بر این، دانشجویانی که کارکردن با دستگاه الکترود قطرهای جیوه را دشوار میدانند، ممکن است مسیر آزمایش را از دست بدهند.

- 2.الکترود فیلم جیوه (MFE)
جایگزینی برای الکترود قطره جیوه، الکترود فیلم جیوه (MFE) است. یک الکترود دیسک کربن شیشه ای در یک محلول آزمایش که حاوی مقداری نیترات جیوه (II) است قرار می گیرد، سپس با نگه داشتن الکترود در پتانسیل منفی کافی، یک لایه نازک از جیوه سطح آن را می پوشاند. MFE ساخته شده به این روش برای استفاده در آزمایش ولتامتری عاری سازی مناسب است، و مقدار کم جیوه درگیر، خطر کمتری دارد.
الکترود پلاتین
با وجود هزینه های مربوط به این فلز گرانبها، پلاتین یکی از پرکاربردترین مواد برای ساخت الکترودهای کاری است.
-
پلاتین فلزی است که به راحتی ماشینکاری می شود
-
از نظر الکتروشیمیایی خنثی است.
-
در سیستم های حلال آبی، الکترود کاری پلاتین در هنگام کار با پتانسیل مثبت انتخاب خوبی است، اما در پتانسیل های منفی، تداخل ناشی از کاهش یون هیدرونیوم یک مشکل است.
-
در سیستمهای حلال آلی بیآب، پلاتین بهترین انتخاب برای الکترود کار میباشد، زیرا دریچه پتانسیل در هر دو جهت مثبت و منفی گسترده است.

- ماکروالکترودهای پلاتین
این الکترودها با قطر بزرگ عموماً با جوش دادن یک دیسک پلاتین ضخیم به انتهای میله برنجی، ماشینکاری دیسک پلاتین و میله برنجی به گونه ای که متحدالمرکز باشند، و سپس قرار دادن یک روکش تفلون در اطراف کل مجموعه ساخته می شوند.
سپس سطح پلاتین با استفاده از یک خمیر پولیش که حاوی ذرات آلومینا زیر میکرون است، به یک سطح با کیفیت آینه ای تبدیل می شود. مانند تمام الکترودهای فلزی جامد، سطح باید گهگاه مجدداً پرداخت شود تا آلایندههای سطحی که در طول آزمایشها جمعآوری شدهاند حذف شوند.
- میکروالکترودهای پلاتین
الکترودهای دیسک پلاتین با قطر کوچکتر و میکروالکترودهای پلاتین معمولاً با پوشاندن طول کوتاهی از سیم پلاتین در شیشه نرم ساخته می شوند. قطر دیسک پلاتین به دست آمده با قطر سیم استفاده شده برابر است. به دلیل سختی پوشش شیشه ای، این الکترودها معمولاً با استفاده از خمیر پولیش که حاوی ذرات الماس زیر میکرون است تا سطح آینه ای شدن صیقل داده می شوند.
الکترود کار پلاتین یک انتخاب عالی برای آزمایشگاه است.
-
در میان الکترودهای فلزی جامد، به دلیل کاربرد آن در طیف گسترده ای از سیستم های الکتروشیمیایی، قطعاً محبوب ترین است.
-
بادوام و ماندگار است و حتی به یک دانشجوی کارشناسی می توان نحوه صیقل دادن صحیح آن را در صورت نیاز آموزش داد.
-
عیب اولیه آن این است که در پتانسیل های منفی در محلول های آبی کاربرد محدودی دارد.
الکترود طلا
الکترودهای کار طلا در امتداد همان خطوط الکترودهای کار پلاتین طراحی می شوند. طلا معمولاً ارزانتر از پلاتین است، اما از نظر الکتروشیمیایی خنثی نیست. سطح یک الکترود طلا در معرض اکسیداسیون با پتانسیل های مثبت متوسط است و بنابراین به طور کلی به اندازه پلاتین مفید نیست.

الکترود کربن
اشکال مختلفی از کربن به عنوان مواد الکترود کار استفاده می شود.
-
الکترودهای کربن روی یک پنجره پتانسیل نسبتاً گسترده در هر دو جهت مثبت و منفی مفید هستند.
-
مزیت اصلی آنها نسبت به الکترودهای پلاتین توانایی کار در پتانسیل منفی بیشتر در محلول های آبی است.
الکترودهای کربن جامد معمولاً از کربن شیشهای یا گرافیت پیرولیتیک ساخته میشوند که هر دو مواد نسبتاً گرانقیمتی هستند که ماشینکاری آنها از پلاتین یا طلا دشوارتر است. سطح الکترود کربن معمولاً باید مرتباً صیقل داده شود، و گاهی اوقات سطح باید با روشهای تجربی مختلف “فعال” شود تا حداکثر کارایی از الکترود حاصل شود.

یک الکترود کربن ارزانتر را میتوان با استفاده از خمیر کربن ساخت. یک فرورفتگی استوانه ای در یک کفه تفلون سوراخ شده و یک کنتاکت الکتریکی در پشت فرورفتگی قرار می گیرد.
هر بار که قرار است از الکترود استفاده شود، فرورفتگی با خمیری که حاوی ذرات کربن است پر میشود و سپس خمیر به دقت صیقل داده میشود تا سطح دیسکی صافی پیدا کند. کار با الکترود خمیر کربنی از نظر فنی سختتر است، زیرا خمیر را میتوان بهطور ناخواسته پس از صیقل دادن خرد کرد.

الکترود دوار
دسته خاصی از تکنیکهای الکتروشیمیایی، که به روشهای هیدرودینامیکی معروف هستند، در واقع شامل استفاده از الکترودهای در حال چرخش هستند.بنابراین الکترودهای دوار یکی از وسایل آزمایشگاه شیمی در آزمایش های الکتروشیمی هستند.
به طور معمول، یک الکترود کربن شیشه ای یا دیسک پلاتین با طراحی ویژه به انتهای یک شفت صلب متصل می شود و سپس این شفت بر روی یک موتور با سرعت بالا نصب می شود. این الکترودها در محلول آزمایشی غوطه ور می شوند و با چندین هزار چرخش در دقیقه می چرخند و یک الگوی “گرداب مانند” در نتیجه حرکت الکترود ظاهر می شود.
از آنجایی که محلول دائماً هم زده می شود، محلول آنالیت تازه همیشه به ناحیه نزدیک به سطح الکترود منتقل می شود. این جریان ثابت آنالیت به آنچه که به عنوان “جریان حالت پایدار” شناخته می شود اجازه می دهد تا در الکترود دوار جریان یابد زیرا آنالیت ها اکسیده یا کاهش می یابند.
اندازه گیری جریان های حالت پایدار معمولاً بسیار آسان است زیرا نسبت به زمان ثابت می مانند. (در اکثر روشهای الکتروشیمیایی دیگر، جریانها با گذشت زمان از بین میروند، زیرا منبع آنالیت نزدیک الکترود تمام میشود.)
(جهت مطالعه در خصوص چیستی الکترودهای دوار کلیک کنید)

حجم سلول هنگام استفاده از الکترود دوار:
هنگام استفاده از یک الکترود دوار، مهم است که حجم سلول به اندازه کافی بزرگ باشد تا جریان محلول به سرعت در حال چرخش را حفظ کند. همچنین دهانه بالای سلول باید به اندازه کافی برای شفت الکترود دوار بزرگ باشد.
این بدان معنی است که محتویات سلول به هوا باز است و حذف اکسیژن را دشوار می کند. هر زمان که از یک الکترود دوار برای مطالعه یک سیستم الکتروشیمیایی حساس به هوا استفاده شود، یک جریان قوی از گاز بی اثر برای پوشاندن محلول مورد نیاز است.
تماس الکتریکی با یک الکترود دوار معمولاً با برس هایی که در تماس مکانیکی با شفت دوار هستند انجام می شود. اگر برس ها یا شفت کثیف باشند، نتایج تجربی توسط یک منبع نویز سریع اما دوره ای پنهان می شود. اگر این اتفاق بیفتد، برس ها را باید در صورت نیاز تمیز یا تعویض کنید.
الکترود مرجع
پتانسیل یک الکترود کار در آزمایش ولتامتری همیشه با توجه به برخی استانداردها کنترل می شود و آن استاندارد الکترود مرجع است.
در حالی که مقیاس ترمودینامیکی پتانسیلهای نیمهواکنش موجود در اکثر کتابهای درسی، پتانسیل الکترود را در برابر الکترود مرجع «هیدروژن استاندارد» (SHE) اندازهگیری میکند، در عمل SHE برای استفاده بسیار دشوار است. به همین دلیل، تعدادی الکترود مرجع دیگر ساخته شده است.
اندازهگیریهای تجربی پتانسیل در برابر این الکترودهای مرجع جایگزین انجام میشود، و سپس پتانسیلها با جمع یا تفریق ساده «تصحیح» میشوند و در برابر SHE گزارش میشوند.
انواع الکترود مرجع
برای مثال چند مدل از انواع الکترودهای مرجع شامل موارد زیر است:
-
الکترود مرجع کالومل اشباع (SCE)
- الکترود مرجع Ag/AgCl یا نقره-کلرید نقره
الکترود کالومل
یکی از رایج ترین الکترودهای مرجع برای کار در محلول های آبی، الکترود کالومل اشباع (SCE) است. نیمه واکنشی که در یک مرجع SCE رخ می دهد در زیر آورده شده است.
در دمای 25 درجه سانتی گراد، پتانسیل رسمی نیمه واکنش SCE 0.2415 ولت مثبت تر از الکترود مرجع SHE است. یک پتانسیل اندازه گیری شده در برابر استفاده از SCE را می توان در مقابل SHE به سادگی با افزودن 0.2415 ولت به آن گزارش کرد.
الکترود SCE باید در یک قطعه شیشه ای مناسب ساخته شود که بتواند مقدار کمی جیوه را در تماس مستقیم با خمیر جامد کالومل (Hg2Cl2) نگه دارد و در عین حال خمیر را با محلول آبی اشباع کلرید پتاسیم در تماس نگه دارد.
نماد کوتاه برای نیم سلول الکترود مرجع کالومل SCE به شرح زیر است:
تماس الکتریکی با فرو بردن یک سیم پلاتین در جیوه مایع ایجاد می شود و محلول کلرید پتاسیم تماس یونی را با محلول آزمایش در سلول الکتروشیمیایی از طریق یک پل نمکی یا فریت شیشه ای متخلخل حفظ می کند.
چنین الکترودهایی را می توان “در خانه” ساخت یا از تولید کنندگان مختلف خریداری کرد.

الکترود مرجع Ag/AgCl یا نقره-کلرید نقره
سایر الکترودهای مرجع مفید مبتنی بر نیمه واکنشهای شامل یک الکترود نقره هستند. برای کار در سیستم های آبی، مرجع “نقره-کلرید نقره” یا “Ag/AgCl” بسیار محبوب است. نیمه واکنش برای این الکترود مرجع به شرح زیر است:
پتانسیل واقعی فرض شده توسط مرجع Ag/AgCl تنها به فعالیت آنیون کلرید بستگی دارد. (دو گونه دیگر که در نیمه واکنش ظاهر می شوند، جامداتی هستند که همیشه فعالیت واحد دارند.)
برای اینکه به عنوان مرجع عمل کند، فعالیت کلرید باید ثابت بماند.
برای انجام این کار، یک سیم نقره (پوشیده شده با لایه ای از کلرید نقره) در محلول داخلی اشباع شده با کلرید پتاسیم غوطه ور می شود. غلظت یون کلرید در حد اشباع ثابت باقی می ماند.
نماد کوتاه برای این نیم سلول الکترود مرجع در زیر آورده شده است:
تماس الکتریکی با اتصال مستقیم به سیم نقره ای ایجاد می شود و محلول الکترود داخلی از طریق یک پل نمکی یا شیشه متخلخل در تماس یونی با محلول آزمایش قرار می گیرد.

الکترود کمکی
در سلولهای دو الکترودی سنتی که فقط یک الکترود کار و یک الکترود مرجع دارند، هر زمان که اندازهگیری انجام میشود، لزوماً جریان از طریق الکترود مرجع عبور میکند.
- اشکال سل دو الکترودی:
اگر جریان کافی از یک الکترود مرجع عبور کند، ترکیب شیمیایی داخلی آن ممکن است به طور قابل توجهی تغییر کند و باعث شود که پتانسیل آن از مقدار استاندارد مورد انتظار دور شود.
به این دلیل و دلایل دیگر، انجام اندازه گیری های الکتروشیمیایی بدون عبور جریان از الکترود مرجع مطلوب است.
- دلیل استفاده از الکترود کانتر:
پتانسیواستاتهای سه و چهار الکترودی مدرن از یک مدار بازخورد برای جلوگیری از این اتفاق استفاده میکنند، اما این مدار بازخورد مستلزم آن است که یک الکترود کمکی اضافی به سلول الکتروشیمیایی وارد شود.
این الکترود کمکی (الکترود کانتر یا شمارنده) مسیری جایگزین برای عبور جریان فراهم می کند، به طوری که تنها جریان بسیار کمی از الکترود مرجع عبور می کند.
انواع الکترود کمکی
الکترود کمکی را می توان تقریباً از هر ماده ای با استفاده از هر هندسه الکترود دلخواه ساخت.
انتخاب های طراحی معمولاً بر اساس یافتن ماده ای است که:
-
از نظر شیمیایی در محلول آزمایشی خاص مورد مطالعه بی اثر است
-
سطح بالایی داشته باشد.
برای مثال:
- در بیشتر موارد، سیم پیچی از سیم پلاتین استفاده می شود،
در محلول های غیر خورنده که تداخل کاتیون های فلزی نگران کننده نیست:
- سیم فولادی ضد زنگ،
- مس
- آلومینیوم
نیز استفاده می گردد.
اگر سلول الکتروشیمیایی از فلز ساخته شده باشد، ممکن است از خود سلول به عنوان وسیله کمکی استفاده شود.از آنجایی که جریان در الکترود کمکی جریان دارد، فرآیندهای الکتروشیمیایی نیز در آنجا رخ می دهد. اگر الکترود کار چیزی را کاهش دهد، الکترود کمکی باید چیزی را اکسید کند و بالعکس.
- جایگاه الکترود کمکی:
محصولات تولید شده در الکترود کمکی، اگر به طرف الکترود کار منتشر شوند، ممکن است در اندازه گیری تجربی اختلال ایجاد کنند. هنگامی که این مشکل وجود دارد، الکترود کمکی در محفظه ای جداگانه حاوی محلول الکترولیت قرار می گیرد که از طریق یک فریت شیشه ای با محلول آزمایش اصلی در تماس یونی است.
با این حال، در بیشتر موارد، کمکی را می توان درست در محلول آزمایش به همراه الکترودهای مرجع و کار قرار داد.