آشنایی با پلاروگرافی و الکترود جیوه
یک الکترود مفید برای مطالعه ولتامتری در محلول راکد الکترود قطره جیوه (DME)، شامل یک ردیف پیوسته از قطرات ریز جیوه است و این قطرات تحت فشار از یک لوله موئین شیشه ای خارج می شوند. ولتامتری در DME را پلاروگرافی می گویند.
درپلاروگرافی الکترود کار شکل قطرات جیوه ریز را به خود می گیرد. این قطرات از یک لوله موئین شیشه ای ظریف یعنی “الکترود قطره جیوه ” خارج میشوند.
dropping mercury electrode
معایب الکترود قطره جیوه
- نیازمند به کار گیری مخزن جیوه مرتفع است.
- در پتانسیل های مثبت جیوه اکسید میشود.
مزایای الکترود قطره جیوه
- به علت تجدید مداوم قطرات الکترود ← لایه انتشار نازک باقی می ماند و غلظت هرگونه فلز احیا شده محلول در جیوه نمیتواند به حد قابل توجهی برسد.
- به علت افتادن قطره و تعویض آن، مواد در سطح آن متراکم نمیشود و سطح الکترود تکرار پذیر است ← آلودگی سطح الکترود در اثر جذب سطی تاثیری ندارد.
- فوق پتانسیل بسیار بالایی برای احیای آب به هیدروژن نشان می دهد ← امکان پلاروگرافی خیلی از یون های فلزی با پتانسیل احیا در محدوه -2 ولت نسبت به کالومل اشباع وجود دارد.
آزمایش پلاروگرافی
در یک سل سه الکترودی داریم:
- الکترود کار ← قطره جیوه (DME)
- الکترود کمکی ← پلاتین
- الکترود رفرنس ← کالومل اشباع (SCE)
الکترود قطره جیوه با یک لوله قابل انعطاف به یک مخزن جیوه مرتفع متصل شده است.
- با طراحی مدار الکترونیک پتانسیل به تدریج تغییر می کند. این فرآیند با استفاده از پتانسیواستات پیشرفته ما قابل انجام است، که دقت و پایداری پلاروگرافی را تضمین میکند.
- هر قطره در پتانسیلی با اندازه چند ده میلی ولت منفی تر از پتانسیل قطره پیشین تشکیل می شود.
- افتادن هر قطره در اثر ضربه چکش همزمان با تغییر پتانسیل صورت میگیرد.
- پتانسیل قطره در تمام طول عمر آن ثابت است.
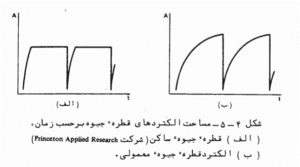
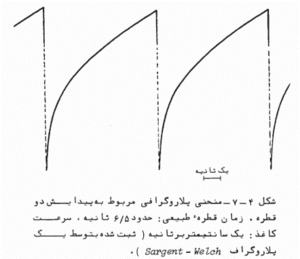
پلاروگرام
فشردگی پر رنگ در نمودار1 ← نتیجه افتادن متوالی قطرات جیوه است که در اثر آن:
-
مساحت سطح الکترود،
-
شدت جریان
تا حدود صفر کم می شود.
با افزودن قطعه الکترونیکی موسوم به مدار نمونه بردار ← فشردگی را می توان حذف کرد (منحنی 2)
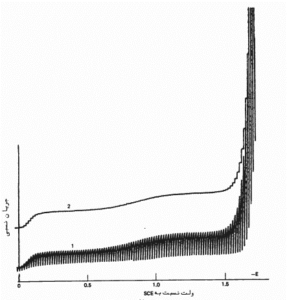
تاثیر خارج ساختن اکسیژن
شکل زیر تغییرات پلاروگرام با خروج اکسیژن را نشان می دهد.
پیک مشاده شده در نمودار مربوط به احیای کاتدی اکسیژن است. با دمیدن گاز بی اثر مانند:
-
ازت
-
فرئون-12
اکسیژن خارج می شود –> فرآیند تخلیه
باتوجه به مشاهده اثر اکسیژن در شکل، ااکسیژن را از تمام محلول ها قبل از پلاروگرافی خارج می کنند.
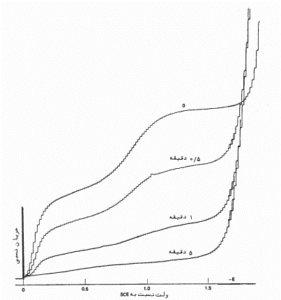
DC پلاروگرام
- درعدم حضور ماده الکترواکتیو
وقتی ماده الکترواکتیو در محیط وجود ندارد:
شکل پلاروگرام شدیدا فشرده منحصرا به اثرات باردار شدن لایه دوگانه مربوط است.
- تغییر چشمگیر در پتانسیل V -0.5 منطبق بر نقطه بار صفراست که تمایلی به تشکیل لایه دوگانه باردار وجود ندارد و جریانی عبور نمیکند.
- در نقاط واقع در دوسوی این نقطه، جریان های گذرا برای باردار کردن ظرفیت خازنی لایه دوگانه ولی با علامت مخالف هم از مدار می گذرند.
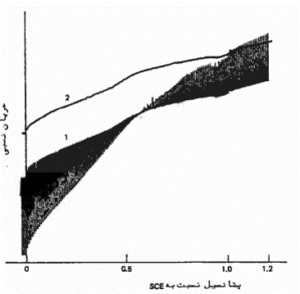
با افتادن قطره، بار متراکم شده در قطره جیوه دفعتا زائل شده و جریان گذرای تازه ای دوباره ظاهر میشود.
با نمونه برداری از جریان درست قبل از افتادن قطره منحنی2 به دست می آید که شکل آن :
- در پتانسیل های مثبت تراز نقطه بار صفر، شکل قسمت بالایی منحنی 1
- در پتانسیل های منفی تر از نقطه بار صفر، شکل زیرین منحنی 1
است.
با تغییر تدریجی در سطح مشترک الکترود و محلول ظرفیت خارنی لایه دوگانه تغییر میکند که مقدار آن:
- در پتانسیل های منفی تر از نقطه بار صفرحدود 20uF برای هرسانتیمتر مربع سطح الکترود
- در پتانسیل های مثبت تراز نقطه بار صفرحدود دوبرابر مقدار گفته شده حالت قبل است.
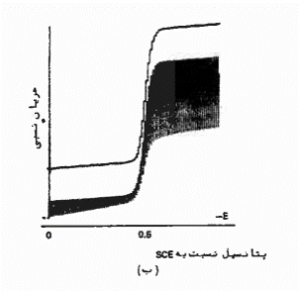
2. پلاروگرام در حضور گونه الکترواکتیو
در حضور گونه الکترواکتیو، پیک در پتانسیلی نزدیک به پتانسیل استاندارد ظاهری به وجود می آید.
در پتانسیل منفی تر از 0.4V- در این مثال، گونه احیا و جریان فارادی مشاهده میشود.
الکترود قطره جیوه ساکن
اگردر الکترود قطره جیوه جریان جیوه با تنظیم زمان قطع شود، مثلا 100 هزارم ثانیه جریان یافته بعد قطع شود:
در این شرایط قطره اندازه ثابت خود را حفظ کرده و تحت تاثیر کشش سطحی به طور آویزان در نوک قطره لوله مویین قرار میگیرد تا اینکه جدا شده و با قطره دیگری جایگزین شود.
مزیت الکترود قطره جیوه ساکن SMDE :
- اندازه گیری ها را روی قطره با سطح ثابت میتوان انجام داد.
- دشواری ناشی از پیدایش متناوب جریان باردار لایه دوگانه در الکترود معمولی را مرتفع می کند.
- مزایای مربوط به تجدید قطره جیوه را حفظ می کند.
فرآیندها در سطح الکترود قطره جیوه
X+ne↔Red
گونه احیا شده در جیوه حل میشود.پتانسیل واکنش از رابطه زیر محاسبه میگردد.
- غلظت های مشخص شده با S مقادیر مربوط به سطح الکترود در هر دو سوی سطح مشترک است در حالیکه فلز احیا شده در طرف جیوه قرار می گیرد.
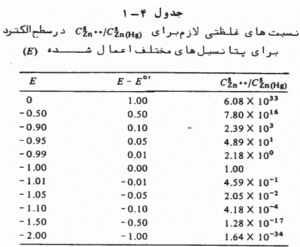
برای مثال:
Zn2++2e↔Zn
با مشخص بودن E0’=-1.7 و n=2 نسبت غلظت ها را برای پتانسیل ها میتوان حساب کرد.
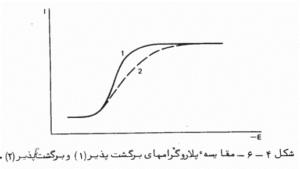
شکل پلاروگرام در سیستم برگشت پذیر و برگشت ناپذیر
1.سیستم برگشت پذیر
- در پتانسیل کم منفی:
تمام گونه در شکل اکسیدی اولیه است(ازمایش با ترکیبی در شکل اکسیدی شروع میشود) درحالیکه در جهت مقابل در سطح الکترود جسم الکترواکتیو در حالت اکسیدی وجود ندارد.
- پتانسیل بسیار منفی:
غلظت روی در ملقمه بالا میرود و جریان بزرگی انتظار میرود.
این شدت جریان تنها توسط انتشار کنترل میشودکه معادل با قبول برگشت پذیری سیستم الکتروشیمیایی است
و در نتیجه آن یک سکو در منحنی ظاهر میشود.
2.سیستم برگشت ناپذیر
در این حالت جریان ابتدایی و انتهایی تفاوت نمی کند.
- در پتانسیل+:
دو منحنی بر هم منطبق اند زیرا کار شیمیایی کمی لازم است و جریان مورد نیاز آن به راحتی قابل وصول است.
- در پتانسیل –:
فوق پتانسیل کافی اعمال شده تا واکنش مبادله الکترون به سرعت پیش رود.
- میان این دو حد پتانسیل:
انتشار میتواند رسیدن ماده احیا شونده بر سطح الکترود را سریعتر از فراهم شدن الکترون ها انجام دهد و در نتیجه شکل زیر حاصل گردد.
اثر الکترولیت حامل در پلاروگرافی
مزایای الکترولیت حامل:
-
افزایش هدایت الکتریکی و کاهش افت اهمی
-
تشکیل لایه دوگانه به صورت تکرار پذیر
-
عدم تغییر ضرایب فعالیت گونه ها (نیروی یونی در حد ثابت نگهداشته میشود.)
-
حذف جریان مهاجرت.
معادلات پلاروگرافی
رابطه ایلکوویچ
این معادله رابطه بین شدت جریان و غلظت گونه الکترواکتیو را میدهد.
دما در رابطه کاترل و ایلکوویچ به صورت آشکار وارد نمیشود اما اثر گذار است:
- ضریب انتشار به دما وابسته است.
- خواص فیزیکی جیوه به دما وابسته است.
با افزایش هر درجه دما مقدار جریان انتشار به میزان 1 تا 2 درصد(در غیاب عوارض سینتیکی) افزایش می یابد.
به همین علت تنظیم دمای ظرف پلاروگرافی با تقریب 0.5 درجه در اندازه گیری کمی، مجاز است.
در عمل رابطه موجود بین غلظت و جریان انتشار به صورت تجربی با کمک محلول استاندارد انجام میشود.
- id جریان انتشار جریانی که درست پیش از پایان عمر هر قطره از مدار میگذرد.
- M برحسب گرم بر ثانیه
- T بر حسب ثانیه
- D برحسب سانتی متر مربع بر ثانبه
- به جای t میتوان τ (زمان قطره) را قرار داد.
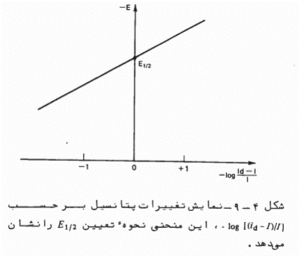
رابطه هیروفسکی ایلکوویچ
شکل منحنی جریان فارادی برحسب پتانسیل از رابطه هیروفسکی ایلکوویچ به دست می آید.
طبق تعریف عملی پتانسیل نیمه موج (E1/2 ) پتانسیلی است که در آن که I=id/2 باشد.
برای واکنش برگشت پذیر نسبت ضرایب انتشار بندرت بیشتر از 2 است (پتانسیلی کمتر از20mv). با جایگذاری این مقدار E1/2 معمولا با E0’ چندان متفاوت نیست.
اگر با گونه الکترواکتیو کمپلکس تشکیل شود اختلاف چشمگیر بین E1/2 با E0’ ایجاد می شود.
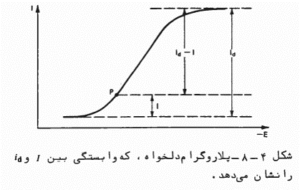
رسم log((id-I)/I)– بر حسب E
شکل منحنی فوق به صورت زیر است:
-
خطی مستقیم با شیب 0.0592/n در دمای 25 درجه.
-
صفر را در E1/2 قطع می کند.
-
N و E1/2 در سیستم برگشت پذیرتعیین میشود.
پلاروگرافی در سیستم برگشت ناپذیر
تفاوت واکنش برگشت پذیر و برگشت نا پذیر مربوط است به:
- در k0 ( ثابت سرعت ناهمگن واکنش)
- Kd ثابت سرعت انتشار
شرایط برگشت پذیری:
با مقادیر متداول در پلاروگرافی:
E1/2 پتانسیلی است که شدت جریان با نصف جریان انتشار برابر شود. در حالت برگشت ناپذیر E1/2 متناسب با زمان قطره تغییر میکند.
بررسی برگشت ناپذیری
E3/4 و E1/4 پتانسیل های وابسته به id ¼ و ¾ است.
- با دانستن برگشت نا پذیری واکنش،n محاسبه میشود.
- با داشتن n بررسی برگشت پذیری واکنش محاسبه میشود.
منابع:


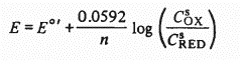
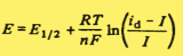

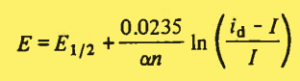
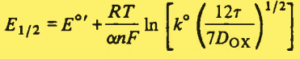
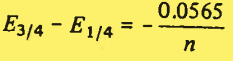
1 نظر
به گفتگو بپوندید و نظر خود را به ما بگویید.
مقاله خیلی خوبی بود. با تشکر