تست های پایداری الکترود شبه مرجع
در این مقاله روش های مطالعه پایداری الکترودهای مرجع غیرآبی و الکترود شبه مرجع مورد بررسی قرار میگیرد. این روش ها شامل آزمایش پتانسیل مدار باز (open circuit potential (ocp)) و آزمون های ولتامتری چرخه ای (CV) هستند. با این آزمون ها ترکیب های متفاوتی از شیشههای متخلخل (frit) و محلول های الکترولیت پرکننده و همچنین اندازه های متفاوتی از لوله های شیشه ای بررسی می شود.
بررسی پایداری pseudo reference electrode(الکترود شبه مرجع)
به طور خاص، دو الکترود مرجع در این سند بررسی و مورد بحث قرار گرفتهاند:
-
الکترود شبه مرجع Ag Low Profile با frit سرامیکی
-
الکترود شبه مرجع Ag سایز استاندارد با frit سرامیکی .
الکترود و محلول های پرکننده متفاوتی در این سند بررسی و گزارش شده است (نگاه کنید به: جدول 1).
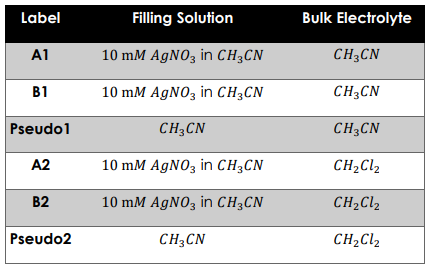
تست های پایداری pseudo reference electrode
ولتاژ مدار باز جهت بررسی پایداری الکترود شبه مرجع
با آزمایش پتانسیل مدار باز (OCP)، پایداری یک الکترود مرجع را می توان در برابر الکترود مرجع دیگر اندازه گیری کرد.
الکترود مرجع (frit|(اشباع)𝐴g|𝐴gCl/KCl)، دارای پتانسیل ردوکس بسیار پایدار در حلال های قطبی مانند استونیتریل است و OCP آن با زمان تغییر نمی کند.
برای آزمایش پایداری الکترودهای مرجع ساخته شده در جدول1 الکترود مرجع: ( frit|(اشباع)𝐴g|𝐴gCl/KCl)، به عنوان یک الکترود اصلی در نظر گرفته می شود که سایر پتانسیل ها را می توان به آن ارجاع داد. بنابراین، اگر تغییری درOCP مشاهده شود، میتوان این تغییر را صرفاً به ناپایداری در الکترود مرجع مورد آزمایش ربط داد.
توجه شود با کاهش قطبیت حلال، یک رانش (دریفت) پتانسیل اتصال مایع بالا در سطح مشترک آبی/غیر آبی به وجود میآید که پتانسیل ردوکس الکترود مرجع ( frit|(اشباع) 𝐴g|𝐴gCl/KCl) را ناپایدار میکند. بنابراین، فقط الکترودهای مرجعی که از استونیتریل، هم برای حلال الکترولیت حجیم و هم برای حلال الکترود مرجع A1 ، B1 و Pseudo1 استفاده میکنند، میتوانند به این روش با الکترود مرجع پایدار (frit|(اشباع)𝐴g|𝐴gCl/KCl) مقایسه شوند تا پایداری آنها تعیین شود (جدول 1)
وقتی OCP الکترودهای مرجع A1، B1 و C1 در برابر (frit|(اشباع)𝐴g|𝐴gCl/KCl) اندازه گیری می شوند، مشخص می شود که هر سه، پتانسیل پایدار با نرخ رانش کمتر از 𝑚V/𝑚in 0.3 را نشان می دهند (شکل 2). بنابراین، frit های مختلف آزمایش شده در اینجا (مینی سرامیک، شیشه ریز، یا سرامیک) ( mini-ceramic, fine glass, ceramic)، هیچ اثر قابل توجهی بر روی پایداری الکترود مرجع ندارند.
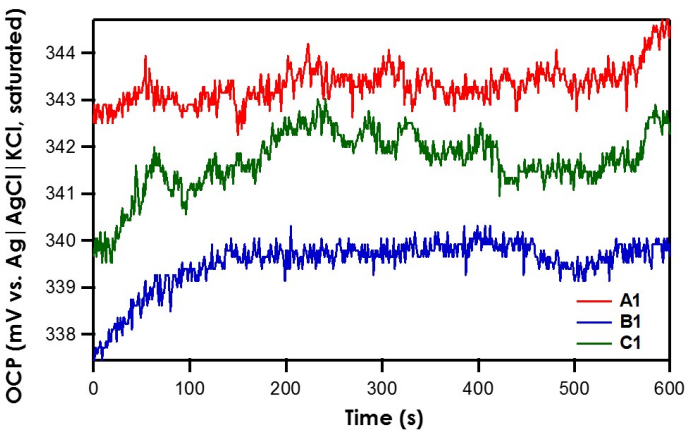
به یاد داشته باشید که A1، B1 ،C1 مخفف (Ag|AgNO3 in CH3CN 10mM |frit ) است. مقادیر گزارش شده برای ( AgNO3 in CH3CN 10mM |frit |Ag) در مقابل (frit|(اشباع)𝐴g|𝐴gCl/KCl) 345 mV است. پتانسیل هر سه الکترود مرجع درحدود 10𝑚V± از مقادیر گزارش شده است که نشان می دهد هر سه الکترود مرجع پایدار هستند.
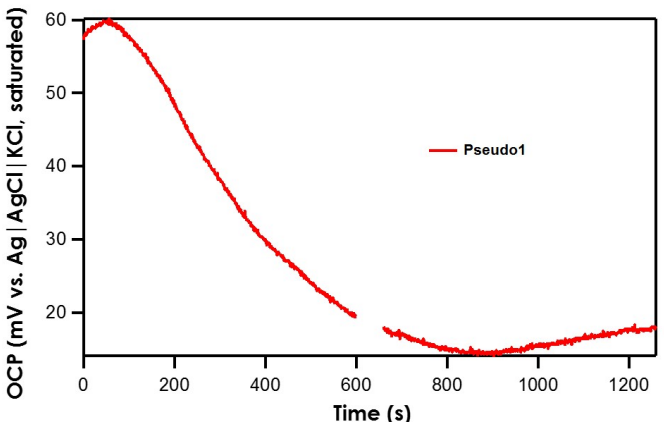
الکترود مرجع Pseudo1 دارای علامت مختصر (𝐴g|𝐴g2𝑂|frit) است. واکنش (اکسید نقره/نقره) پتانسیل ردوکس پایداری ندارد. بنابراین، وقتی Pseudo1 OCP در برابر (frit|(اشباع)𝐴g|𝐴gCl/KCl) اندازه گیری می شود ‘در ابتدا دریفت های بزرگ پتانسیل (~5mV/min) تا زمان تثبیت، مشاهده می شود (شکل 3). بنابراین، ضروری است که الکترودهای شبه مرجع حداقل یک ساعت قبل از استفاده در محلول متعادل شوند.
آزمون ولتامتری چرخه ای جهت بررسی الکترود شبه مرجع
تست های OCP فروسن تحت یک فرض کلیدی عمل می کنند: پتانسیل یکی از الکترودهای مرجع تغییر نمی کند. بنابراین، باوجود این که امکان ایجاد ثبات نسبی بین دو الکترود مرجع با آزمایش OCP وجود دارد، نمی توان تشخیص داد که آیا هر دو الکترود با سرعت یکسان در حال رانش(دریفت) هستند یا خیر.
یک آزمایش ولتامتری چرخه ای (CV) با استفاده از فروسن تست های OCP را تعریف می کند. فروسن تحت یک اکسیداسیون برگشت پذیر و یک الکترونی قرار می گیرد تا فروسنیوم را تشکیل دهد (معادله1). پتانسیلی که در آن اکسیداسیون رخ می دهد نسبتاً ثابت است و یک آزمایش شیمیایی مستقل برای سنجش رانش الکترود مرجع ایجاد می کند (یعنی اگر پیک اکسیداسیون بین CV ها جابجا شود، به رانش در الکترود مرجع نسبت داده می شود).
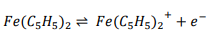
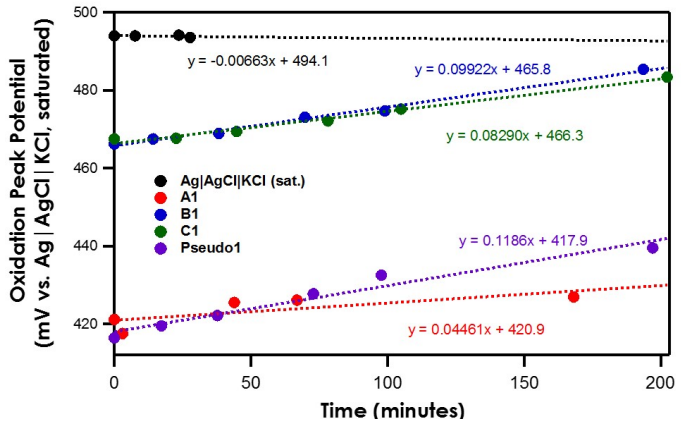
فروسن ( 10mM) به محلول های الکترولیت حجیم که قبلا در جدول 1 نشان داده شده است اضافه می شود. ولتاموگرام های چرخه ای با استفاده از یک سیم پیچ پلاتین به عنوان الکترود کار، یک الکترود کمکی و یک الکترود مرجع به دست می آید. سپس پتانسیل پیک اکسیداکتیو فروسن به عنوان تابعی از زمان برای هر الکترود مرجع اندازه گیری می شود.
هنگامی که حلال محلول الکترولیت حجیم استونیتریل است، رانش(دریفت) (frit|(اشباع)𝐴g|𝐴gCl/KCl) (بسیار کم است، کمتر از 0.01𝑚V/min (نگاه کنید به شکل 6).
هر سه الکترود مرجع Ag|AgNO3 in CH3CN 10mM |frit ) (A1، B1، C1)) دارای نرخ رانش(دریفت) کمتر از min /mV 0.1 هستند.
با این حال، از مطالب قبل به یاد بیاورید که پتانسیل الکترود کار در برابر الکترود مرجع اندازه گیری می شود و پتانسیل الکترود مرجع به تعادل واکنش پایدار آن بستگی دارد. از آنجایی که تعادل واکنش پایدار در A1، B1 و C1 اکسیداسیون برگشت پذیر نقره به نیترات نقره است، پتانسیل اکسیداسیون فروسن باید در پتانسیل یکسانی برای هر سه الکترود مرجع رخ دهد. با این حال، برای تطبیق مینی سرامیکی A1 frit ، از یک الکترود کارمتفاوت استفاده می شود و یک اختلاف پتانسیل پیک اکسیداسیون 𝑚V 50~ ایجاد می کند.
در حالی که پتانسیل پیک اکسیداسیون نسبی بین A1 با B1 و C1 متفاوت است، همه آنها هنوز در یک سری داده بسیار پایدار هستند.
در نهایت، با حداقل ده دقیقه انتظار پس از ساخت Pseudo1، نرخ رانش آن به کمتر از 0.2𝑚M/𝑚in کاهش می یابد.
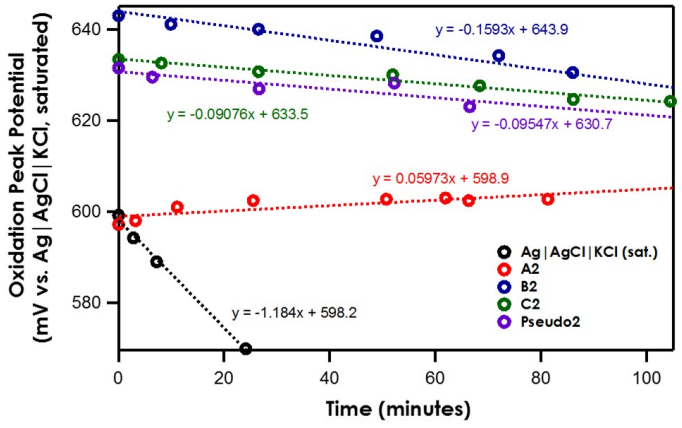
هنگامی که محلول الکترولیت حجیم، دی کلرومتان است، پایداری (frit|(اشباع)𝐴g|𝐴gCl/KCl) به دلیل رانش پتانسیل اتصال عظیم القا شده در فصل مشترک آب/دی کلرومتان بسیار کاهش می یابد (نگاه کنید به شکل 5). نرخ رانش A2، B2، C2 و Pseudo2 کمتر از 𝑚V/𝑚in 0.2 است که نشان دهنده پایداری قوی است.
پایدارترین الکترود مرجع غیرآبی
در حالی که مطمئناً رانش های بزرگ ( 𝑚V/𝑚in1) به دلیل ناپایداری یک الکترود مرجع است، منشاء رانش های کوچک (کمتر از 𝑚V/𝑚in0.2) مشاهده شده در استونیتریل و دی کلرومتان مشخص نیست.نمی توان این را رد کرد که شیمی ردوکس فروسن با انجام اسکن های CV مکرر دستخوش تغییرات ظریفی شود.
- به عبارت دیگر، رانش می تواند به دلیل تغییر پتانسیل اکسیداسیون ناشی از تغییرات در الکتروشیمی سطح یا وضعیت سطح الکترود باشد.
- علاوه بر این، محصول اکسیداسیون فروسنیوم در حلال آلی پایدارتر است. یک لایه نازک از محصولات واکنش جانبی فروسنیوم می تواند سطح الکترود را مسدود کند و باعث تغییر در موقعیت پیک شود.
پایدارترین الکترود مرجع غیرآبی ( Ag|AgNO3 (10mM) in 100 mM 𝑁𝐵4𝑃𝐹6CH3CN |frit) با نرخ رانش کمتر از𝑚V/S 0.1 است. توصیه می شود که یک الکترود مرجع غیرآبی روزانه با استفاده از یک جفت ردوکس شناخته شده مانند فروسن در محلول استاندارد (𝑚M 1-5 فروسن در mM100 𝑚𝑁𝐵4𝑃𝐹6 𝐶𝐻3𝐶) کالیبره شود.
در حالی که الکترود مرجع نقره/نیترات نقره پایدارترین است، محققان باید هنگام استفاده از آن احتیاط کنند. از آنجایی که یون های نقره در استونیتریل محلول هستند، می توانند از frit عبور کرده و محلول توده را آلوده کنند. برای به حداقل رساندن نشت یون نقره، می توان از double junction استفاده کرد.
با این وجود، در کاربردهای خاصی مانند مطالعه کاتالیز تکامل هیدروژن، حتی مقدار کمی از آلودگی یون نقره، پتانسیل کاهش اسید را تغییر میدهد و دادههای بهدستآمده برای کاتالیزور مورد نظر را پیچیده میکند. در این موارد، بهتر است از یک الکترود شبه مرجع استفاده شود.
یک الکترود شبه مرجع محلول الکترولیت حجیم را آلوده نمی کند. با این حال، رانش پتانسیل بیشتری را تجربه می کند. برای توضیح این موضوع، الکترود شبه مرجع باید حداقل یک ساعت قبل از استفاده به تعادل برسد و به یک استاندارد داخلی مانند فروسن ارجاع داده شود. در صورت امکان، پیک های ردوکس فروسن باید در هر ولتاموگرام حلقوی گرفته شده گنجانده شود، یا مستقیماً پس از یک آزمایش جابجایی خطی اندازه گیری شود.
تنظیمات آزمایش بررسی الکترود شبه مرجع:
تنظیم آزمایشی برای انجام اندازهگیریهای الکتروشیمیایی، یک سلول الکتروشیمیایی با پنج پورت (نگاه کنید به شکل 7) برای آزمایشهای ولتامتری چرخهای فروسن استفاده شد :
-
یک پورت برای یک الکترود کمکی،
-
یکی برای الکترود کار (30 𝑐m سیم پیچ پلاتین با mm0.5 قطر)
-
و سه درگاه دیگر برای الکترودهای مرجع (نوع (B) - fine glass frit ، نوع (B)- Pseudo fine glass frit ، و نوع (C) - standard size ceramic frit)
برای آزمایشهای پتانسیل مدار باز، از سه پورت برای الکترود کار استفاده شد:
- نوع (B) – fine glass frit ،
- نوع (B)- Pseudo fine glass frit ،
- نوع (C) – standard size ceramic frit
والکترود مرجع ( frit|(اشباع) 𝐴g|𝐴gCl/KCl ) فقط یک پورت را اشغال می کرد والکترود کمکی ثابت باقی ماند.

به منظور آزمایش پایداری mini-ceramic frit (نوع (A))، تنظیم دیگری استفاده شد که از یک الکترود چاپ شده با صفحه نمایش برای الکترودهای کار و کمکی آن استفاده می کرد (نگاه کنید به: شکل 6).

(جهت دسترسی به متن لاتین مقاله کلیک کنید.)
(جهت مطالعه در مورد الکترودهای مرجع غیر آبی، کلیک کنید.)

